Содержание статьи
Введение
Ингибиторы натрий-глюкозного котранспортера 2 типа (ИНГТ2) продемонстрировали значимые кардиоваскулярные преимущества у пациентов с сахарным диабетом 2 типа (СД2) как с установленными сердечно-сосудистыми заболеваниями, так и с множественными факторами риска таковых [1–3]. Было выдвинуто несколько теорий, объясняющих положительное влияние ИНГТ2 на сердечно-сосудистые исходы. Так, в исследованиях получены данные по снижению преднагрузки на сердце вследствие усиления натрийуреза, улучшению метаболизма кардиомиоцитов, снижению выраженности фибротических и воспалительных процессов в миокарде и сосудистой стенке [4–6]. Однако данная тема продолжает оставаться предметом активного изучения.
Cахарный диабет 2 типа ассоциирован с развитием хронического воспаления вследствие действия различных механизмов. При этом показано, что ИНГТ2 могут снижать уровни некоторых цитокинов, таких как фактор некроза опухоли α, интерлейкин-6, высокочувствительный С-реактивный белок (вчСРБ) [7]. Кроме того, хорошо известно, что фибротические процессы в миокарде развиваются у пациентов с СД2 независимо от наличия артериальной гипертензии и выраженности коронарного атеросклероза [8]. В связи с этим изучение процессов фиброза и воспаления у пациентов с СД2 является актуальным.
Цель исследования: оценить динамику уровня сывороточных маркеров, ассоциированных с процессами фиброза и воспаления при СД2, на фоне лечения дапаглифлозином.
Материал и методы
Проведено одноцентровое проспективное исследование, одобренное этическим комитетом ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. До вступления в исследование все пациенты подписывали информированное согласие. Включали пациентов с СД2 длительностью более 1 года, уровнем гликированного гемоглобина от 7% до 10%, без верифицированной атеросклеротической болезни сердца и сосудов, но с множественными факторами риска сердечно-сосудистых событий (дислипидемией, ожирением, артериальной гипертензией). Кроме того, критериями включения были возраст от 40 до 65 лет, стабильная сахароснижающая, гиполипидемическая и антигипертензивная терапия как минимум в течение 12 нед. до включения в исследование. В исследование не включали пациентов с фибрилляцией предсердий, клапанными пороками сердца, ревматологическими заболеваниями, обострением хронических заболеваний, сахарным диабетом 1 типа, симптомами гипотензии и уровнем систолического артериального давления (САД) ниже 95 мм рт. ст., уровнем N-концевого пропептида натрийуретического гормона (NT-proBNP) >125 нг/мл, скоростью клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 и хронической болезнью почек, заболеваниями печени а также получающих инсулинотерапию, терапию глюкокортикостероидами, антагонистами минералокортикоидных рецепторов. Пациенты получали дапаглифлозин в дозе 10 мг/сут в течение 6 мес. в дополнение к базовой терапии СД2.
В ходе исследования проводили забор образцов крови до начала лечения дапаглифлозином и через 6 мес. лечения. Образцы крови забирали натощак (после 8 ч голодания), оценивали следующие показатели: гликированный гемоглобин (HbA1c), аланинаминотрансферазу, аспартатаминотрансферазу, креатинин, липидограмму (общий холестерин, липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП), триглицериды), NT-proBNP, вчСРБ, галектин-3, тканевой ингибитор матриксных металлопротеиназ-1 (TIMP-1), матриксную металлопротеиназу-9 (MMP-9), стимулирующий фактор роста, экспрессируемый геном 2 (ST2), карбокситерминальный фрагмент проколлагена I типа (PIСP). Уровень вчСРБ определяли на анализаторе Cobas Integra 400+ иммунотурбидиметрическим методом. Концентрацию NT-proBNP определяли электрохемилюминесцентным методом c применением тест-системы Elecsys (Roche Diagnostic). Оценку сывороточных уровней галектина-3 (R&D system), ММР-9 и TIMP-1 (R&D system), sST2 (Clinical diagnostics, Presage ST2 kit), PICP (USCN Life Science) проводили методом иммуноферментного анализа. Кроме того, в начале и в конце исследования оценивали массу тела, рост, окружность талии, уровень артериального давления (АД). С целью оценки нормальных значений биомаркеров фиброза в исследование дополнительно были включены 15 пациентов сходного возраста без СД2 и других хронических заболеваний, в том числе сердечно-сосудистых и заболеваний почек (группа контроля).
Для статистического анализа использовали программу SPSS Statistics. Количественные данные представлены в виде медианы и 25-го и 75-го квартилей — Me [Q25; Q75], качественные признаки — в виде абсолютного и относительного (%) показателей. Различия между количественными показателями выявляли с помощью критерия Вилкоксона. Корреляционный анализ проводили с использованием рангового коэффициента корреляции Спирмена. Нулевая гипотеза отвергалась при р<0,05.
Результаты исследования
В исследование включено 27 пациентов (возраст 56 [49; 61] лет), у большинства из которых были СД2 длительностью более 4 лет (7 [4; 12] лет) и ожирение
I степени. Базовая сахароснижающая терапия включала комбинацию метформина с препаратами сульфонилмочевины или ингибиторами дипептидилпептидазы 4 типа (иДПП-4).
Основная характеристика пациентов и динамика изучаемых маркеров фиброза и воспаления представлена в таблице 1. За 6 мес. лечения дапаглифлозином наблюдалось значимое снижение уровня HbA1c с 8,2 [7,6; 8,8]% до 7,8 [7,2; 8,1]% (р=0,001), снижение ИМТ и уменьшение окружности талии. За время наблюдения не отмечено значимых изменений содержания липопротеинов и триглицеридов, СКФ и АД.
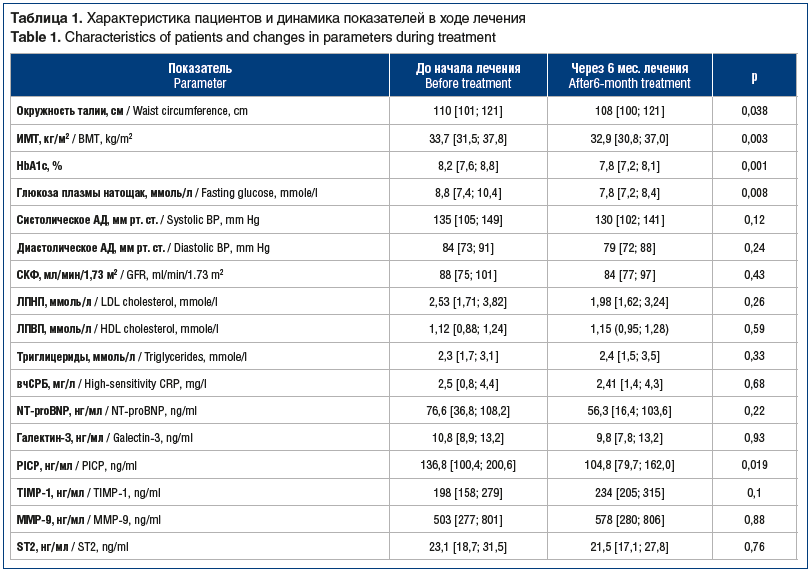
Содержание вчСРБ и NT-proBNP не отличалось от нормальных значений и не претерпело статистически значимых изменений по прошествии 6 мес. лечения дапаглифлозином. Исходно пациенты имели значимо бóльшие концентрации галектина-3, PICP и MMP-9 по сравнению с группой контроля (p=0,017, p=0,006 и p=0,008 соответственно). При оценке динамики содержания галектина-3, MMP-9, TIMP-1, ST2 не было получено значимых различий с исходными значениями (см. табл. 1). В то же время через 6 мес. лечения дапаглифлозином наблюдалось статистически значимое снижение концентрации PICP с 136,8 [100,4; 200,6] нг/мл до 104,8 [79,7; 162,0] нг/мл (р=0,019) и повышение концентрации TIMP-1 с 188 [138; 270] нг/мл
до 234 [205; 315] нг/мл (р=0,011).
Обсуждение
Преобладание синтеза коллагена I типа над его деградацией приводит к накоплению в миокарде избытка волокон коллагена и указывает на процесс фиброза, который происходит в интерстициальном и периваскулярном пространстве, в том числе при диабетической кардиомиопатии [9]. Уровни PICP, который является маркером образования и деградации коллагена I типа, надежно коррелируют с объемом образующегося коллагена как у пациентов с хронической сердечной недостаточностью (ХСН), так и без таковой [9].
В исследованиях показано, что концентрации PICP выше у пациентов с СД2, чем у пациентов без СД2 [10]. Сходные различия были продемонстрированы и в нашем исследовании. Терапия дапаглифлозином в течение 6 мес. приводила к значимому снижению уровня P1CP по сравнению с исходным. Сходная динамика была получена в исследовании другого ИНГТ2 у пациентов с СД2 и очень высоким риском сердечно-сосудистых событий [11].
В нашем исследовании не установлено значимого снижения концентраций NT-proBNP на фоне лечения дапаглифлозином в течение 6 мес., что можно объяснить включенной в исследование популяцией пациентов без ХСН и без высоких концентраций NT-proBNP. Поскольку NT-proBNP является маркером ХСН и его уровень коррелирует с ее тяжестью, даже в исследованиях пациентов с СД2 и ХСН с сохранной фракцией выброса не было выявлено значимого снижения концентрации NT-proBNP [12]. Тем не менее исследование DAPA-HF продемонстрировало, что риск ухудшения течения ХСН или смерти от сердечно-сосудистых заболеваний был ниже в группе дапаглифлозина, чем в группе плацебо [13]. Таким образом, несмотря на ограниченное влияние на уровень NT-proBNP, ИНГТ2 улучшают клинические исходы у пациентов с ХСН, что говорит о несоответствии между краткосрочными изменениями уровней NT-proBNP и клиническими исходами.
Концентрации ST2, вчСРБ, MMP-9 и ее ингибитора TIMP-1 значимо не изменились на фоне терапии дапаглифлозином, что согласуется с данными других исследований [11, 14, 15]. Вероятно, отсутствие значимой динамики показателей ряда маркеров в ходе нашего исследования связано с тем, что пациенты без ХСН и сердечно-сосудистых событий находятся на том этапе сердечно-сосудистого континуума, когда концентрации маркеров не могут в полной мере отражать тяжесть и прогноз у данных пациентов, а их изменения не могут быть зафиксированы за 6-месячный период наблюдения. Кроме того, отсутствие отрицательной динамики содержания данных биомаркеров может говорить о замедлении воспалительных и фиброзных процессов, имеющих место при СД2, и потенциально реализовываться в улучшении сердечно-сосудистых исходов. Также стоит принимать во внимание наличие ожирения и других неучтенных факторов, которые могут влиять на значения оцениваемых нами маркеров.
Заключение
Терапия дапаглифлозином в течение 6 мес. приводила к снижению уровня PICP, что наряду с другими механизмами может свидетельствовать о положительном воздействии дапаглифлозина на сердечно-сосудистые и почечные исходы у пациентов с СД2. Требуется проведение дальнейших проспективных исследований с более длительным наблюдением на больших выборках для детального изучения динамики фибротических процессов и отражающих их биомаркеров. Кроме того, представляется целесообразным проведение оценки процессов фиброза у двух различных групп пациентов с СД2 — с сердечно-сосудистыми событиями в анамнезе и с факторами риска таких событий.
Сведения об авторах:
Лебедев Денис Андреевич — младший научный сотрудник НИЛ диабетологии ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России; 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2; ORCID iD 0000-0003-1808-1331.
Бабенко Алина Юрьевна — д.м.н., заведующая НИЛ диабетологии ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России; 197341, Россия, г. Санкт-Петербург, ул. Аккуратова, д. 2; ORCID iD 0000-0002-0559-697X.
Контактная информация: Бабенко Алина Юрьевна, e-mail: alina_babenko@mail.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 18.02.2021.
Поступила после рецензирования 18.03.2021.
Принята в печать 12.04.2021.
About the authors:
Denis A. Lebedev — junior researcher of the Research Laboratory of Diabetology, V.A. Almazov National Medical Research Center; 2, Akkuratov str., St. Petersburg, 197341, Russian Federation; ORCID iD 0000-0003-1808-1331.
Alina Yu. Babenko — Dr. Sc. (Med.), Head of the Research Laboratory of Diabetology, V.A. Almazov National Medical Research Center; 2, Akkuratov str., St. Petersburg, 197341, Russian Federation; ORCID iD 0000-0002-0559-697X.
Contact information: Alina Yu. Babenko, e-mail: alina_babenko@mail.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 18.02.2021.
Revised 18.03.2021.
Accepted 12.04.2021.
.
Информация с rmj.ru






