Липидснижающая терапия у пациентов с высоким риском сердечно-сосудистых осложнений
Содержание статьи
Введение
Сердечно-сосудистая патология, к которой относят инсульты, инфаркты миокарда, продолжает лидировать по показателям смертности, потери трудоспособности взрослого населения. Согласно опубликованным данным ВОЗ, около 30% случаев смерти среди взрослого населения планеты происходят по причине сердечно-сосудистых заболеваний (ССЗ), основными механизмами запуска которых являются нарушение липидного обмена, атеросклеротические изменения сосудистой стенки и атеротромбоз [1].
Подобная ситуация характерна и для нашей страны, где, по данным Всероссийского научного общества кардиологов, ССЗ ежегодно уносят жизни около 1,3 млн человек, являются причиной смерти более 50% россиян. В целом в РФ более чем у 23 млн человек выявлены заболевания сердечно-сосудистой системы (ССС), среди которых инсульты (как ишемические, так и геморрагические), ИБС, гипертоническая болезнь [2]. На долю ИБС приходится 51% смертей от ССЗ, цереброваскулярной патологии (инсульты) — более 27% [3, 4].
Основная роль в запуске механизмов развития и прогрессирования ССЗ отводится так называемым факторам риска (ФР), приводящим к формированию патологических изменений ССС. Термин «фактор риска» используется в медицинской практике почти 70 лет. В последнее время насчитывается свыше 200 ФР ССЗ, список которых пополняется ежегодно. Деление ФР на немодифицируемые и модифицируемые имеет исключительно практическое значение, поскольку позволяет определить возможность коррекции патологического состояния [5]. Снижение заболеваемости и смертности от ССЗ возможно только при своевременном выявлении ФР, эффективном терапевтическом воздействии на них.
Для оптимизации выбора тактики терапевтического воздействия на ФР принято выделять несколько групп пациентов с ранжированным риском ССЗ. Первую группу (высокого и очень высокого риска) составляют лица с различными клиническими манифестациями ИБС, атеросклерозом периферических и церебральных артерий, аневризмой брюшного отдела аорты. К этой же группе риска относят больных с наличием нескольких ФР, но не имеющих клинически манифестированных вышеперечисленных заболеваний, при этом по шкале SCORE (Systematic Cоronary Risk Evaluation — Европейская шкала для расчета риска смерти от ССЗ) 10-летний риск смерти составляет свыше 5%. При наличии сахарного диабета (СД) 1 или 2 типа, в частности, осложненного микроальбуминурией, пациента относят к группе высокого и очень высокого риска ССЗ.
В настоящее время СД рассматривается как глобальная эпидемия, поскольку прогноз на 2030 г. относительно увеличения количества больных СД до 511 млн подтверждается, и уже на 2015 г. число пациентов с верифицированным СД достигло 415 млн (данные International Diabetes Federation (IDF) — Международной федерации диабета) [6]. Изменилась и характеристика фенотипа СД 2 типа (СД2) — сегодня это лица молодого возраста (до 40 лет), что приводит к более раннему появлению осложнений в виде развития ССЗ [6, 7].
Выбор адекватной и эффективной тактики терапии и профилактики с целью снижения риска ССО у пациентов высокого и очень высокого риска является одним из основных направлений политики государства в сфере здравоохранения.
Патофизиологические механизмы, развивающиеся в организме больного СД2, выражены в гликозилировании различных белков и биологически активных молекул, среди которых холестерин липопротеидов низкой плотности (ХС ЛПНП), имеющий высокую сенситивность к свободным радикалам. Эти субстраты в условиях хронической гипергликемии характеризуются более выраженными атерогенными свойствами [3]. Данные механизмы приводят к типичным изменениям показателей липидного спектра при СД2, которые проявляются гипертриглицеридемией, повышением концентрации атерогенной фракции ХС ЛПНП и снижением доли холестерина липопротеидов высокой плотности (ХС ЛПВП). Именно наличие представленных патологических особенностей нарушения липидного обмена во многом обусловливает раннее развитие макрососудистых осложнений при СД2 [5]. Превентивные меры по снижению риска развития ССО у лиц очень высокого и высокого риска должны быть направлены как на изменение образа жизни, так и на выбор эффективной фармакологической стратегии, включающей препараты, корригирующие углеводный и липидный обмен, антигипертензивную терапию и антитромбоцитарные средства.
Коррекция липидного обмена — одна из важнейших составляющих выбора превентивных мер по снижению ССО, несомненно, статины являются единственной группой лекарственных средств с доказанной эффективностью. Однако без ранжирования пациентов по уровню суммарного сердечно-сосудистого риска и уровня ХС ЛПНП на группы риска невозможно достичь максимального превентивного эффекта. При высоком риске ССО, повышении ХС ЛПНП до 1,8–2,5 ммоль/л пациентам наряду с изменением образа
жизни одновременно должна быть назначена гиполипидемическая терапия. При повышении ХС ЛПНП выше 2,5 ммоль/л фармакологическая коррекция нарушений липидного обмена проводится немедленно. Также решение о немедленном назначении статинов принимается в случае показателя ХС ЛПНП ≥1,8 ммоль/л у пациентов с очень высоким риском ССО. Контроль эффективности липидснижающей терапии проводится на основании достижения целевых уровней основных показателей липидного обмена: общего холестерина (ОХ), триглицеридов (ТГ), ХС ЛПНП и ХС ЛПВП. Согласно результатам крупных исследований эффективности и безопасности длительного применения статинов, доказано их мощное действие в отношении профилактики цереброваскулярных заболеваний и ИБС у пациентов с СД2 [8].
Однако в реальной клинической практике непрерывный длительный прием статинов бывает ограничен высокой стоимостью последних, что нередко приводит к прекращению жизненно необходимой терапии.
Именно эта проблема явилась причиной проведения проспективного наблюдательного исследования с оценкой эффективности и безопасности, а также сопоставимости действия дженерического розувастатина в лечении больных с высоким риском ССО. Целью исследования стало определение эффективности терапии розувастатином в программе первичной профилактики ССО посредством оценки показателей не только липидного обмена, но и сосудисто-тромбоцитарного гемостаза у пациентов с верифицированным СД2 и наличием дислипидемии.
Материал и методы
Оценивали показатели липидного спектра в сыворотке крови: ОХ, ХС ЛПНП, ХС ЛПВП, ТГ, определяли уровни концентрации молекулярных маркеров активации тромбоцитов (пластиночный фактор-4 (4ПФ), β-тромбоглобулин (β-ТГ)), а также фактора фон Виллебранда (ФВ) как маркера дисфункции эндотелия у 50 больных СД2. Все показатели оценивали в динамике на протяжении 420±15 дней терапии розувастатином. Провели анализ сопоставимости липидснижающего и плейотропного гемостазиологического эффекта в условиях замены оригинального розувастатина на дженерический препарат (в аналогичных дозах — использовали 10 мг/сут). Дизайн исследования: проспективное наблюдательное исследование безопасности, эффективности розувастатина и сопоставимости с референтным препаратом у группы больных с высоким сердечно-сосудистым риском (ССР) при первичной профилактике ССС. Исследуемая группа включала 50 больных СД2, АГ, дислипидемией, церебральным атеросклерозом (гемодинамически незначимым, подтвержденным допплерографией). Старт терапии статинами начинали с оригинального розувастатина в дозе 10 мг, впоследствии осуществляли перевод больных на дженерический препарат (Розукард®) в дозе 10 мг. Смену препаратов проводили на визите 3 в сроки 112±7 дней от начала приема статина.
Результаты исследования и их обсуждение
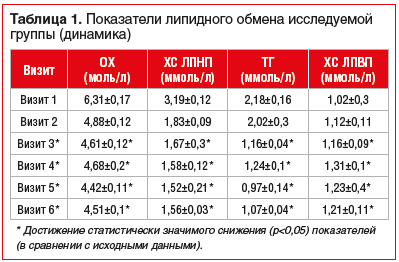
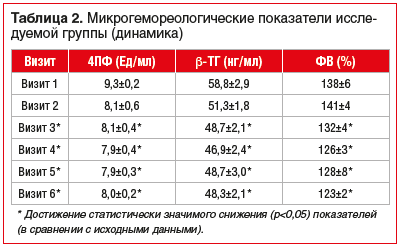
Оценку лабораторных показателей проводили на старте терапии, затем каждые 2 мес. (56±7 дней от предыдущего визита) в течение 8 мес., затем финальную оценку лабораторных параметров в среднем через 1,5 года от начала приема розувастатина (табл. 1 и 2).
С позиции доказательной медицины показана безусловная необходимость длительной терапии статинами, входящими в структуру так называемой базисной терапии первичной и вторичной профилактики ССО у лиц высокого и очень высокого риска. Определены и доказаны в исследовании JUPITER возможные механизмы, отвечающие за протективный эффект статинов по предупреждению инсультов. Одним из них, несомненно, является мощный липидснижающий эффект, приводящий к снижению скорости прогрессирования атеросклеротического процесса, уменьшению размеров атеросклеротической бляшки, в т. ч. в системе каротидных артерий. Кроме того, наличие доказанных дополнительных (плейотропных) эффектов приводит к снижению дисфункции эндотелия сосудов, уменьшению неспецифического воспаления, стабилизации атеросклеротической бляшки. Нейропротективное действие ГМГ-КоА-редуктазы было показано в ряде экспериментальных работ [9, 10]. Крупные клинические исследования (COMETS, LUNAR, MERCURY–I, SOLAR, STELLAR) показали преимущественную эффективность розувастатина в сравнении с другими представителями этой фармакологической группы. Назначение стартовой дозы розувастатина 10 мг/сут уже снижало уровень ХС ЛПНП более чем на 40%.
В эксперименте продемонстрировано влияние статинов на процессы тромбообразования, уменьшение гиперактивации тромбоцитов [10–12].
В нашем наблюдении проведена оценка динамики ОХ, ХС ЛПНП, ХС ЛПВП, ТГ, а также маркеров активации тромбоцитов и эндотелиального повреждения у лиц, относящихся к группе высокого риска макрососудистых осложнений с СД2 и дислипидемией, при назначении им в рамках первичной профилактики ССО розувастатина 10 мг/сут. В результате наблюдения отмечено, что спустя 3 мес. непрерывного приема розувастатина появились значимые позитивные изменения уровней ХС ЛПНП, ХС ЛПВП, ТГ и снижение концентрации 4ПФ, β-ТГ а также ФВ — основного маркера дисфункции эндотелия (в рамках нашего наблюдения). Таким образом, результаты нашего исследования не противоречат данным, полученным в крупных многоцентровых рандомизированных клинических исследованиях, о высокой эффективности розувастатина в условиях хронической гипергликемии и дислипидемии.
В силу объективных обстоятельств (чаще финансово-экономический фактор) на 3-м визите пациентам меняли оригинальный розувастатин на дженерический в сопоставимой дозе — 10 мг/сут. Анализ эффективности дженерического препарата по влиянию на показатели липидного спектра и сосудисто-тромбоцитарного гемостаза показал, что при переводе пациентов с терапии оригинальным препаратом на аналогичную дозу дженерического достигнутые стабильные целевые значения контролируемых показателей не изменились, нежелательные явления не возникли.
Заключение
Подводя итог, необходимо отметить, что пациенты, входящие в группу высокого риска ССО, имеющие СД2, показывают ухудшение адаптационных механизмов, что проявляется ухудшением баланса липидных показателей и изменением основных микрогемореологических маркеров. Как следствие этих процессов, происходит усиление агрегационной активности тромбоцитов, дисфункции эндотелия. В этом контексте и согласно полученным нами результатам цель терапии состоит не только в достижении стойкого снижения уровня ХС ЛПНП и поддержании его на целевом уровне в зависимости от группы риска ССО, но и в запуске позитивных плейотропных механизмов эндотелиопротекции и микрогемореологии. То, насколько улучшатся эти показатели, во многом зависит от генерации препарата, в этом смысле розувастатин имеет благоприятный профиль безопасности с прогнозируемым эффектом снижения ХС ЛПНП в зависимости от дозы. Необходимо помнить, что максимальный терапевтический эффект развивается, как правило, не ранее 4–6 нед. с начала применения. Несомненным правилом в терапии статинами должно быть соблюдение непрерывного (при отсутствии нежелательных явлений) курса лечения, поскольку только такой подход приводит к снижению сердечно-сосудистого риска [9–11]. Достижение максимальной приверженности лечению розувастатином возможно с учетом подбора оптимального по соотношению эффективности и безопасности дженерического препарата Розукард®.
Информация с rmj.ru






