Хронический запор: этиология и возможности терапии
С.С. Вялов
Клиника Global Medical System, г. Москва
Цель обзора: рассмотрение проблематики запора, являющегося наиболее частой гастроэнтерологической жалобой в общей популяции.
Основные положения. В статье приведены современные сведения об этиологии хронических запоров, проанализированы диагностические подходы, дана сравнительная характеристика основных групп препаратов, применяемых при лечении запоров. Изложены подробные рекомендации по тактике ведения пациентов, выбору препарата для конкретного пациента с учетом особенностей клинической картины.
Подбор терапии запора — сложная задача, требующая взаимодействия врача и пациента. Лечение хронического запора должно начинаться с патогенетической терапии, направленной на нормализацию частоты дефекаций и консистенции стула. Злоупотребление «народными» средствами может приводить к усугублению патологического процесса.
Заключение. Запор остается одной из ключевых проблем гастроэнтерологии, требующей грамотной дифференциальной диагностики, аккуратного подбора терапии при постоянном взаимодействии врача с пациентом.
Ключевые слова: хронический запор, синдром раздраженного кишечника, слабительные, полиэтиленгликоль, калия битартрат.
Запор является наиболее частой гастроэнтерологической жалобой в общей популяции, и во многих случаях в его основе лежат экономические факторы. Запор может быть манифестацией метаболических болезней (сахарный диабет, гипотиреоз, гиперкальциемия), неврологических или обструктивных кишечных заболеваний, но чаще ассоциирован с приемом различных медикаментов.
На сегодняшний день множеством соглашений определены критерии функциональных нарушений кишечника и запоров, в основном исключающие морфологические и биохимические изменения. Поэтому принято различать первичные нарушения, при которых отсутствует органическая патология, и вторичные, сочетающиеся со структурными изменениями кишечника. Однако достоверных маркеров дифференциации функционального нарушения, хронического запора и синдрома раздраженного кишечника нет, и их поиск продолжается [16].
К диагностическим признакам запора относятся присутствие твердого комковатого стула (тип 1-2 по Бристольской шкале) более чем в 25% дефекаций, необходимость натуживания, чувство неполного опорожнения или препятствия в прямой кишке, а также необходимость ручного вспоможения при дефекации [16, 19]. В соответствии с Римскими критериями III, при хроническом запоре у пациента сохраняются два симптома и более в течение 3 месяцев.
Запор как симптом, связанный с нарушением прохождения содержимого по кишечнику, встречается более чем у 20% жителей экономически развитых стран и крупных городов. Частота запоров выше среди женщин и улиц пожилого возраста и достигает 26% среди мужчин и 34% среди женщин в возрасте старше 65 лет [37]. Причем многие люди, страдающие запорами, составляют группу «не пациентов», они не обращаются за помощью к врачам и не учитываются в официальной статистике [37].
Запоры могут развиваться вследствие нарушения передвижения масс по толстому кишечнику и аноректальной области, при этом проксимальные отделы ЖКТ зачастую бывают не затронуты патологическим процессом. Запор с медленным транзитом может быть идиопатическим. Выделяют вторичные запоры, связанные с обструктивной патологией, включающей колоректальный рак, неврологическими и психиатрическими нарушениями, такими как анорексия, а также метаболическими и эндокринными нарушениями, в том числе сахарным диабетом.
Кроме основных диагностических симптомов, могут появляться дополнительные симптомы как следствие длительной задержки стула. Отмечаются распирание или дискомфорт в различных отделах живота и в области ануса [4, 5].
Пациенты указывают на изменение консистенции каловых масс, их уплотнение и фрагментарность, что линейно соотносится со временем транзита содержимого по кишечнику. Для упрощения диалога с пациентом удобно использовать Бристольскую шкалу форм кала, по которой больной сам может определить как форму, так и время транзита по кишке. Зачастую длительная задержка стула может приводить к развитию синдрома избыточного бактериального роста и присоединению условно-патогенной флоры, что проявляется метеоризмом и газообразованием [35].
В связи с изменением скорости и типа транзита содержимого выделяют несколько подтипов идиопатического хронического запора:
- запор с нормальным кишечным транзитом: пациенты предъявляют жалобы на затруднение дефекации и не отвечают на терапию волокнами и слабительными, не имеют нарушений аноректальной зоны, но зачастую реагируют на психосоциальный стресс;
- инертный толстый кишечник: сниженная сократительная активность толстого кишечника в ответ на прием пищи или бисакодила при нормальной активности аноректальной зоны;
- задержка опорожнения: нормальный толстокишечный транзит на фоне отсутствия значимых сокращений прямой кишки;
- диссинергическая дефекация: неэффективная деятельность мышц в связи с нарушением расслабления, несинхронными сокращениями сфинктеров, мышц тазового дна и повышением внутрибрюшного давления.
Важным дифференцирующим клиническим признаком является наличие болевого синдрома. В соответствии с Римскими критериями, хронический запор протекает без болей, в отличие от синдрома раздраженного кишечника с преобладанием запоров (рис. 1). Поэтому для пациентов, имеющих боли в животе, должна быть применена другая тактика наблюдения и лечения [39].
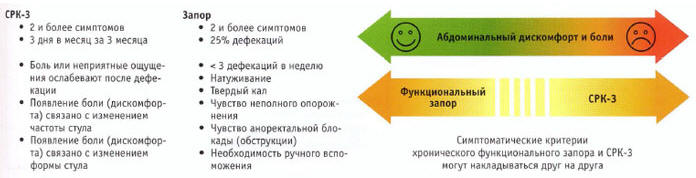
Рис. 1. Римские критерии III для хронического запора и синдрома раздраженного кишечника с преобладанием запоров (СРК-3) [32]
Необходимо помнить о «красных флагах», или «симптомах тревоги», которые могут свидетельствовать о наличии органической патологии или соматоморфного расстройства. Среди данных анамнеза важно уточнить, какие медикаменты принимает пациент, и исключить среди них так называемые запирающие средства. К ним относятся наркотические анальгетики, нейролептики, трициклические антидепрессанты, блокаторы кальциевых каналов, алюминийсодержащие антациды, антипаркинсонические препараты [25].
Короткая продолжительность заболевания и настораживающий анамнез с высокой вероятностью свидетельствуют об органической патологии! Большинство (около 70-80%) пациентов с хроническими запорами не имеют органических нарушений, тогда как малая длительность заболевания возможна при карциноме, депрессии, гипотиреозе. Для более детальной диагностики и подтверждения выявленных изменений необходима консультация проктолога [23].
Всем пациентам старше 50 лет показана однократная колоноскопия. При наличии семейного анамнеза патологии кишечника, полипоза кишечника или колоректального рака колоноскопия показана по достижении возраста 40 лет.
Исключение органической патологии подтверждает диагноз первичного хронического запора, однако требует проведения дополнительной лабораторной и инструментальной диагностики, позволяющей дифференцировать или исключить воспалительный процесс, электролитные нарушения, патологию почек, эндокринные заболевания (табл. 1) [34].
Таблица 1. Лабораторная дифференциальная диагностика хронического запора [1]
| Заболевания | Определяемые показатели |
| Воспалительные заболевания | общий анализ крови + СОЭ; С-реактивный белок (болезнь Крона); фекальный кальпротектин |
| Электролитные нарушения | натрий, калий, кальций (опухоли) |
| Патология почек | креатинин |
| Эндокринные заболевания | глюкоза (сахарный диабет); гликозилированный гемоглобин HbAl; С-пептид; ТТГ, Т3, Т4 (гипотиреоз) |
| Нарушения пищеварения | общий анализ кала; копрограмма; энтеропатогенные бактерии (посев) |
Примечание. СОЭ — скорость оседания эритроцитов, Т — трийодтиронин, Т4 — тироксин, ТТГ — тиреотропный гормон
Инструментальная диагностика подразумевает проведение рентгеновского исследования в прямой или боковой проекции стоя для оценки распределения воздуха и вынесения предположения о локализации обструкции. Рентгеновское исследование может быть дополнено контрастированием. Обструкция или другие структурные изменения со стороны кишечника, а также воспалительные заболевания кишечника подтверждаются результатами колоноскопии, КТ или МРТ. В ряде случаев для исключения нарушений функции мышц тазового дна показаны дефекография, аноректальная манометрия и тест изгнания баллона (баллонный тест). У пациентов с хронической анемией неясного генеза возможно проведение капсульной эндоскопии или интестиноскопии для исключения патологии тонкого кишечника. Капсульная эндоскопия проводится после эндоскопических или контрастных исследований в качестве второго, уточняющего, этапа диагностики (табл. 2).
Таблица 2. Дифференциальная диагностика запоров [1]
| Возможная причина | Дифференциальный диагноз |
|
1. Хронический запор при заболеваниях кишечника |
|
| Хронический привычный запор | недостаток потребления клетчатки, недостаток потребления жидкости, гиподинамия, снижение раздражения при дефекации |
| Синдром раздраженного кишечника | запор — преобладающий симптом |
| Функциональная аноректальная обструкция | дисфункция тазового дна, анизм, синдром нисходящей толстой кишки, пролапс слизистой, ректоцеле |
|
2. Хронический запор как самостоятельный симптом |
|
| Лекарственный запор | анальгетики (опиаты), антигистаминные, спазмолитики, антихолинергические, антидепрессанты и антипсихотики, препараты железа, препараты алюминия (антациды), препараты бария, антагонисты кальция (верапамил), ганглиоблокаторы, антагонисты рецепторов 5-НТ3, нейролептики, цитостатики (алкалоид Барвинка — Vinca) |
| 3. Эндокринные нарушения | гипотиреоз, болезнь Аддисона, гиперпаратиреоидизм |
| 4. Электролитные нарушения | гипокалиемия, гиперкальциемия |
| 5. Системные заболевания | системный склероз, системная красная волчанка, миотоническая дистрофия |
| 6. Беременность | — |
| 7. Психические нарушения | депрессия, анорексия, курительные смеси, наркотики |
|
8. Неврологические нарушения |
|
| Периферические | вегетативная или автономная невропатия, сахарный диабет (диабетическая полинейропатия), болезнь Гиршпрунга, полиневрит Жилиана-Барэ, ганглионевроматоз, болезнь Чагаса |
| Центральные | Спинальные: повреждение периферических нервов, опухоли, рассеянный склероз, диссеминированный энцефаломиелит, Spin a bifida, нейрофиброматоз, синдром Ши-Дрегера, спинная сухотка Tabes dorsalis Церебральные: рассеянный склероз, болезнь Паркинсона, сосудистые заболевания мозга, опухоли мозга |
Тотальное проведение полного спектра обследований для дифференциальной диагностики хронического запорав западной медицинской школе не принято из экономических соображений и ввиду того, что обилие медицинских процедур, направленных на исключение патологии, нарушает качество жизни пациента. Комплекс дифференциальной диагностики показан при наличии «тревожных симптомов» [43]. В число последних входят:
- первое появление после 50 лет;
- ректальное кровотечение;
- усиление симптомов по ночам;
- снижение веса;
- лихорадка или субфебрилитет;
- анемия;
- пальпируемое образование [35].
Лечение хронического запора
Начало работы с пациентом, имеющим хронический запор, должно включать обучение пациента, коррекцию диеты, соблюдение достаточного количества и правильного соотношения растительных продуктов в диете, а также назначение слабительных. При тяжелом запоре может потребоваться консультация хирурга, а ведение пациентов с нормальным или медленным транзитом осуществляют в соответствии с алгоритмом (рис. 2).
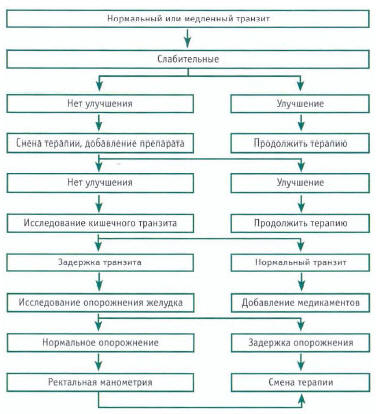
Рис. 2. Алгоритм ведения пациентов с хроническим запором и нормальным или медленным транзитом [9]
Общий подход к лечению хронического запора, безусловно, зависит от данных обследований, свидетельствующих о нормальном или замедленном транзите по кишечнику. Медикаментозное лечение хронического запора начинается со слабительных, увеличивающих объем, и/или размягчающих слабительных или свечей. Эффективность, безопасность, приверженность лечению и стоимость терапии, а также ответ на нее имеют решающее значение при выборе средства для терапии.
Обучение пациента предполагает снижение зависимости от слабительных, акцент на ежедневной дефекации и необходимости потребления достаточного количества жидкости и пищевых волокон. Пациенты должны пытаться осуществить дефекацию после приема пищи, используя естественное постпрандиальное усиление моторики кишечника, особенно в утренние часы, когда моторная активность кишечника выше.
Необходим контроль потребления жидкости пациентом. Допустимым является количество жидкости от 1,5 до 2,5 л, которое должно индивидуально адаптироваться в соответствии с состоянием пациента и с учетом наличия или отсутствия у него сердечно-сосудистых заболеваний или нарушений функции почек. Важное значение придается изменению стиля жизни пациента и увеличению аэробной физической активности без физической нагрузки до 30-60 минут от 3 до 5 раз в неделю [2, 29].
Медикаментозная терапия подразумевает назначение симптоматических и патогенетических средств, а также профилактику развития осложнений. Назначение этиотропного лечения возможно только после постановки окончательного диагноза. В случае первичного запора может быть назначена только патогенетическая терапия [3,11].
Основной целью лечения больных с первичными и вторичными запорами являются нормализация консистенции стула и восстановление пассажа содержимого по кишечнику. Для этого используются препараты различных групп, которые назначаются по ступенчатой схеме (рис. 3) [30, 31].
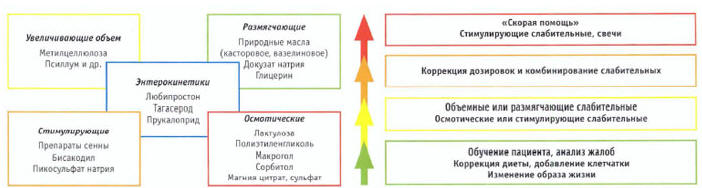
Рис. 3. Слабительные средства, применяемые в лечении запоров [1]
Пищевые волокна, такие как метилцеллюлоза и псиллум, достаточно действенны, в том числе с психологической точки зрения. Принимаемые вместе с большим количеством жидкости, они эффективны у многих пациентов. Показано, что 3-недельная терапии псиллумом и клетчаткой сухофруктов, принимаемыми 3 раза в день, приводит к более полным и самостоятельным актам дефекации на фоне приема клетчатки, улучшает консистенцию стула [7].
Потребление клетчатки может улучшать клиническую картину хронического запора [40]. Волокна злаков обычно представляют собой обработанную клеточную стенку и не перевариваются в кишечнике, задерживая воду. Волокна, содержащиеся в цитрусовых и овощах, стимулируют рост толстокишечных бактерий [8]. Пшеничные отруби являются одним из наиболее эффективных слабительных волокон, но могут провоцировать вздутие и боли в животе у пациентов с синдромом раздраженного кишечника [18].
Существует прямая зависимость между количеством потребляемых волокон, потреблением жидкости и объемом каловых масс. Увеличение количества клетчатки, например злаковых, имеет объемный эффект. Кроме этого, значимый эффект дает рост потребления волокон фруктов и компонентов сахаров (фруктоза, сорбитол), содержащихся в таких продуктах, как яблоки, персики, груши, вишня, изюм, виноград и орехи. Рекомендованное количество пищевых волокон составляет в среднем от 20 до 40 г в сутки. Следует употреблять сырые отруби — от 2 до 6 чайных ложек с каждым приемом пищи, запивая стаканом воды. У некоторых пациентов, особенно с замедленным кишечным транзитом, волокна могут провоцировать вздутие и ощущение распирания, что снижает приверженность лечению примерно на 50%. Пациентам необходимо сообщать об этом нежелательном явлении. Волокна в рацион следует вводить постепенно в соответствии с их переносимостью и эффективностью [6, 33, 36, 41].
Слабительные, увеличивающие объем, или объемные слабительные, включают семена подорожника, метилцеллюлозу, кальция поликарбонафил и пшеничный декстрин. Они представляют собой натуральные или синтетические полисахариды или дериваты целлюлозы, сорбирующие воду в кишке и увеличивающие объем каловых масс. Эти слабительные эффективно повышают частоту дефекаций и увеличивают мягкость стула без значимых побочных явлений. Используются самостоятельно или в сочетании с пищевыми волокнами.
В систематическом обзоре показана эффективность псиллума у пациентов с хроническим запором в отношении увеличения частоты стула и найдена недостаточно доказанной эффективность других форм, таких как метилцеллюлоза, отруби, поликарбофил кальция [10]. Другой обзор продемонстрировал эффективность и безопасность поликарбофила кальция и низкую эффективность метилцеллюлозы и псиллума [38]. Данные исследований по увеличивающим объем слабительным остаются противоречивыми, однако безопасность этих средств позволяет начинать с них терапию [10, 38].
Пациентам, которые имеют плохой ответ на терапию волокнами или плохо переносят волокна, может потребоваться применение других слабительных. Слабительные, размягчающие стул, такие как докузат натрия, предназначены для уменьшения поверхностного натяжения кала, что позволяет воде легче проникать в кал. В качестве монотерапии они менее эффективны, чем другие слабительные. Систематический обзор определил, что размягчающие стул слабительные оказывают меньшее влияние на частоту стула, чем псиллум [42].
В группу осмотических слабительных входят полиэтиленгликоль (ПЭГ), плохо абсорбируемые и неабсорбируемые сахара и солевые слабительные, индуцирующие секрецию воды в просвет кишечника и вызывающие учащение дефекаций. Избыточное использование осмотических слабительных может приводить к электролитным нарушениям у больных с сердечно-сосудистыми заболеваниями или нарушением функции почек [28].
Для лечения запоров доступны растворы ПЭГ и порошки для приготовления раствора (не содержащие электролитов). Систематические обзоры показывают эффективность этих средств в отношении повышения частоты и улучшения консистенции стула. Они принимаются один раз в день со стартовой дозы 17 г и титруются до максимальной дозы 34 г/сут. При отсутствии ответа возможно снижение дозы до 8,5 г с добавлением стимулирующего слабительного ежедневно или каждый третий день [14,15].
Слабительные, основанные на солях магния (магниевое молоко, цитрат магния и сульфат магния), плохо абсорбируются в кишечнике и действуют как гиперосмолярный раствор. Однако у многих пациентов на фоне терапии выявляется гипермагниемия, особенно при нарушении функции почек [17].
Безопасный вариант осмотических слабительных — синтетические дисахариды, лактулоза. Они не метаболизируются ферментами в кишечнике, таким образом, вода и электролиты остаются в просвете кишечника вследствие осмотического эффекта сахаров. Лактулоза требует определенного времени (обычно 24-48 часов) до достижения эффекта, что связано с ее транзитом до толстого кишечника. По данным систематических обзоров, лактулоза оказывает выраженное действие на частоту дефекации и консистенцию стула, проявляет слабительный эффект. Сорбитол имеет схожую эффективность и является менее дорогостоящей альтернативой. И лактулоза, и сорбитол могут вызывать вздутие живота и газообразование. По результатам Кокрановских метаанализов, ПЭГ превосходит лактулозу в эффективности [26].
Стимулирующие слабительные, такие как бисакодил, препараты сенны, пикосульфат натрия, оказывают свое действие за счет нарушения транспорта электролитов через слизистую кишки. Таким образом, они увеличивают сократительную активность. Бисакодил хорошо переносится, однако его прием может вызывать диарею и боли в животе. Продолжительный прием стимулирующих слабительных ассоциирован с гипокалиемией, энцефалопатией, связанной с потерей белка, и с перегрузкой солями [20, 22].
Стимулирующие слабительные после длительного или частого использования вызывают лаксативный синдром и в дальнейшем могут приводить к атонии кишечника. Препараты сенны при длительном приеме также требуют повышения дозы, вызывают псевдомеланоз кишечника, и в связи с данным побочным действием они запрещены или ограничены к применению во многих западных странах. Стимулирующие слабительные у пациентов с хроническим запором могут использоваться лишь периодически во время подбора терапии.
Новые препараты
Линаклотид — минимально абсорбируемый пептид, агонист С-рецепторов к гуанилатциклазе, который стимулирует секрецию жидкости в кишечник и ускоряет транзит. Этот препарат одобрен в США в дозировке 145 мг/сут. Однако роль линаклотида в лечении хронического запора, а также соотношение долгосрочных пользы и риска при его применении не определены. Три исследования показали его эффективность в увеличении частоты дефекаций, но наиболее частый и дозозависимый побочный эффект — диарея — требовал прекращения терапии у 4% пациентов [27].
Любипростон — локальный активатор каналов хлора, обогащающий хлором содержимое кишечника. В исследованиях продемонстрирована эффективность любипростона в увеличении частоты дефекаций, однако имеются сообщения о развитии вздутия, дискомфорта в животе и диареи. Роль любипростона в лечении хронического запора пока неясна и нуждается в изучении, нет сравнительных исследований с другими препаратами, отсутствуют данные о длительной терапии. Изучение препарата затруднено в связи с его высокой стоимостью и индуцированием тошноты у 30% пациентов [21,24].
Мизопростол — аналог простагландина, который успешно используется у некоторых пациентов для лечения тяжелого запора. По результатам исследований, этот препарат может быть эффективен в дозе 200 мкг/сут или через день с повышением дозы на 200 мкг/сут в соответствии с переносимостью недельного курса вместе с ПЭГ в дозе от 17 до 34 г/сут. Однако мизопростол не должен использоваться у беременных, поскольку может индуцировать потерю плода; кроме того, он усиливает менструальные кровотечения [44].
Колхицин также может быть эффективен в лечении хронического запора. Исследования показали увеличение количества дефекаций при терапии колхицином в дозе 0,6-1,0 мг однократно в сутки через 2-3 месяца терапии. Но препарат не может быть использован у пациентов с почечной недостаточностью и вызывает миопатию.
Прукалоприд — прокинетик, взаимодействующий с 5-НТ4-рецепторами, доступен в Европе, Канаде, России, но не зарегистрирован в США. В исследованиях препарат проявлял эффективность в дозах 1-4 мг/сут, превосходил плацебо при терапии в течение 4-12 недель. Прукалоприд безопасен и хорошо переносится пожилыми больными. Пациенты из трех исследований наблюдались в течение 24 месяцев. При этом улучшение качества жизни отмечалось к концу 12 недель терапии и поддерживалось до 18 месяцев. Сравнительное исследование прукалоприда и ПЭГ показало, что ПЭГ не менее эффективен, но имеет преимущество в отношении стоимости лечения [12,13].
Эвакью. В арсенале врача должны присутствовать слабительные, способные стимулировать моторику и предотвращать развитие вторичных симптомов хронического запора, таких как метеоризм или газообразование. В последние годы для лечения хронических запоров появились интересные для клиницистов комбинированные препараты слабительных, которые облегчают период подбора терапии и нейтрализуют вторичные симптомы задержки стула. К таким средствам относятся ректальные суппозитории Эвакью, содержащие натрия бикарбонат, калия битартрат и ПЭГ.
Под действием влаги в ампуле прямой кишки ПЭГ расплавляется, создавая условия для взаимодействия воды с натрия бикарбонатом и калия битартратом. Образующийся углекислый газ растягивает прямую кишку, повторяя физиологический процесс дефекации.
Растяжение гладкой мускулатуры прямой кишки вызывает мышечные сокращения, провоцируя процесс эвакуации каловых масс, а образуемая вода разжижает каловые массы, что облегчает их выведение из организма. Расплавленный ПЭГ действует как смазывающий компонент, способствуя легкому прохождению каловых масс. Обычно дефекация наступает уже в течение 5-10 минут после введения суппозитория.
Препарат в форме свечей эффективнее при большинстве форм хронического запора, в том числе при сочетанной патологии. Наличие нескольких механизмов патогенетического воздействия позволяет применять препарат как для начальных форм запоров, так и при тяжелых и резистентных запорах. Эвакью является безопасным средством, не имеет противопоказаний и может быть рекомендован беременным и при грудном вскармливании, а также при наличии механических повреждений прямой кишки, при анальных трещинах и геморрое.
Заключение
В современных российских условиях доступность медикаментозных средств приводит к видоизменению типичной клинической картины запора, развитию лаксативной болезни, возникновению привыкания к препаратам и рефрактерных запоров. Применение пациентом «популярных», «народных» и прочих альтернативных методов лечения не только не гарантирует выздоровления или уменьшения степени тяжести заболевания, но и, напротив, приводит к усугублению патологического процесса. Все более востребованной становится информационная поддержка пациентов со стороны врачей. Объяснение больному стратегии лечения и последовательности действий способствует улучшению контакта с больным и повышает степень его доверия врачу. Врач должен знать стратегию лечения пациентов с запорами и современные лекарственные препараты.
- У первичных пациентов с хроническими запорами, в особенности имеющих «тревожные симптомы», необходимо проведение тщательной дифференциальной диагностики.
- Лечение хронического запора должно начинаться с патогенетической терапии, направленной на нормализацию частоты дефекаций и консистенции стула. Недопустимо самолечение пациентов непроверенными и «народными» средствами, не имеющими доказательной базы.
- В качестве первой ступени лечения хронического запора следует рассматривать препарат Эвакью, который показал высокую эффективность и безопасность при длительном применении.
Литература
- Вялов С. С. История одного пациента: тактика лечения запора // Эффектив. фармакотерапия в гастроэнтерологии. 2013. № 4 (41). С. 22-29.
- Маев И. В., Вьючнова Е. С., Лебедева Е. Г., Гвинтовкина Т. О. и др. Хронический запор, подходы к постановке диагноза и лечению // Фарматека. 2011. № 12. С. 58-63.
- Минушкин 0. Н., Ардатская М. Д. и др. Хронический запор: представления, патогенез, диагностика, новые возможности лечения // Врач. 2012. №- 12. С. 77-82.
- Парфенов А. И. Эволюция взглядов на патогенез и терапию хронического запора // 2011. № 12.
- Andrews С. N., Storr M. The pathophysiology of chronic constipation //Can. J. GastroenteroL 2011. N25. Suppt. В. Р. В16-21.
- Anti M., Pignataro G., Armuzzi A., Valenti A. et at. Water supplementation enhances the effect of high-fiber diet on stoot frequency and laxative consumption inadult patients with functional constipation // Hepatogastroenterology. 1998. Vol. 45. N21. P. 727-732.
- Attaluri A., Donahoe R., Valestin J., Brown K. et al. Randomised clinical trial: dried plums (prunes) vs. psyllium for constipation // Aliment. Pharmacol. Ther. 2011. Vol. 33. N 7. P. 822-828.
- Badiali D., Corazziari £., Habib F. I, Tomei E. et al. Effect of wheat bran in treatment of chronic nonorganic constipation. A double-blind controlled trial // Dig. Dis. Sri. 1995. Vol. 40. N 2. P. 349-356.
- Bharucha A. E„ Dorn S. D., Lembo A., Pressman A.; American Gastroenterological Association. American Gastroenterological Association medical position statement on constipation // Gastroenterology. 2013. Vol. 144. N 1. P. 211-217.
- Bharucha A. E., Pemberton J. H., Locke G. R. 3rd. American Gastroenterological Association technical review on constipation // Gastroenterology. 2013. Vol. 144. N1. P. 218-238.
- Camilleri M. New treatment options for chronic constipation: mechanisms, efficacy and safety // Can. J. GastroenteroL 2011. N 25. Suppt. В. Р. В29-35.
- Camilleri M., Van Outryve M. J., Beyens G., Kerstens R. et al. Clinical trial: the efficacy of open-label prucalopride treatment in patients with chronic constipation — follow-up of patients from the pivotal studies // Aliment. Pharmacol. Ther. 2010. Vol. 32. N9. P. 1113-1123.
- Cinca R., Chera D., Gruss H. J., Halphen M. Randomised clinical trial: macrogol/PEO 3350+electrolytes versus prucalopride in the treatment of chronic constipation — a comparison in a controlled environment // Aliment. Pharmacol. Ther. 2013. Vol. 37. N 9. P. 876-886.
- Corazziari £., Badiali D., Bazzocchi G, Bassotti G. et al. Long term efficacy, safety, and tolerabilitity of low daily doses of isosmotic polyethylene glycol electrolyte balanced solution (PMF-100) in the treatment of functional chronic constipation // Gut. 2000. Vol. 46. N 4. P. 522-526.
- Dipalma J. A., Cleveland M. V., McGowan J., Herrera J. L. A randomized, multicenter, placebo-controlled trial of polyethylene glycol laxative for chronic treatment of chronic constipation // Am. J. Gastroenterol. 2007. Vol. 102. N 7. P. 1436-1441.
- Drossman D. A. The functional gastrointestinal disorders and the Rome III process // Gastroenterology. 2006. Vol. 130. N5. P. 1377-1390.
- Dupont C, Campagne A., Constant F. Efficacy and safety of a magnesium sulfate-rich natural mineral water for patients with functional constipation // Clin. Gastroenterol. Hepatol. 2014. Vol. 12. N 8. P. 1280-1287.
- Floch M. H., Wald A. Clinical evaluation and treatment of constipation // Gastroenterologist. 1994. Vol. 2.N1.P. 50-60.
- Gray J. R. What is chronic constipation? Definition and diagnosis// Can. J. Gastroenterol. 2011. N25. Suppl. В. Р. В7-10.
- Heizer W. D., Warshaw A. I., Waldmann T. A., taster L. Protein-losing gastroenteropathy and malabsorption associated with factitious diarrhea // Ann. Intern. Med. 1968. Vol. 68. N4. P. 839-852.
- Johanson J. F, Ueno R. Lubiprostone, a locally acting chloride channel activator, in adult patients with chronic constipation: a double-blind, placebo-controlled, dose-ranging study to evaluate efficacy and safety // Aliment. Pharmacol. Ther. 2007. Vol. 25. N11. P. 1351-1361.
- Kamm M. A., Mueller-Lissner S., Wald A., Richter E. et al. Oral bisacodyl is effective and well-tolerated in patients with chronic constipation // Clin. Gastroenterol. Hepatol. 2011. Vol. 9. N 7. P. 577-583.
- Kruis W. Obstipation ats Begleitsymptom und ab inerwunschte Arzneimittelwirkung // S. A. Muller-Lissner, L. M. A. Akkermans. Chronische Obstipation und Stuhlinkontinenz. Springer Verlag, 1989. P. 201-211.
- Lang L. The Food and Drug Administration approves lubiprostone for irritable bowel syndrome with constipation // Gastroenterology. 2008. Vol. 135. N 1. P. 7.
- Lankisch P. 6., Lubbers H., Mahlke R., M’uller С H. Gastroenterologie. Von Symptom zur Diagnose. Ein Leitfaden fur Klinik und Praxis, 2009.
- Lee-Robichaud H., Thomas K., Morgan J., Nelson R. L. Lactulose versus Polyethylene Glycol for Chronic Constipation // Cochrane Database Syst. Rev. 2010. Vol. 7. CD007570.
- Lembo A. J., Schneier H. A., Shiff S. J., Kurtz С. В. et al. Two randomized trials of linaclotide for chronic constipation // N. Engl. J. Med. 2011. Vol. 365. N 6. P. 527-536.
- Lembo A., Camilleri M. Chronic constipation // N. Engl. J. Med. 2003. Vol. 349. N 14. P. 1360-1368.
- Liu L. W. Chronic constipation: current treatment options // Can. J. Gastroenterol. 2011. N25. Suppl. В. Р. В22-28.
- Locke G. R. 3rd, Pemberton J. H., Phillips S. F AGA technical review on constipation. American Gastroenterological Association // Gastroenterology. 2000. Vol. 119. N6. P. 1766-1778.
- Locke G. R. 3rd, Pemberton J. H., Phillips S. F American Gastroenterological Association Medical Position Statement: guidelines on constipation // Gastroenterology. 2000. Vol. 119. N6. P. 1761-1766.
- Longstreth G. F, Thompson W. G, Chey W. D., Houghton L. A. et al. Functional bowel disorders // Gastroenterology. 2006. Vol. 131. N 2. P. 688.
- Muller-Lissner S. A. Effect of wheat bran on weight of stool and gastrointestinal transit time: a meta analysis // Br. Med. J. (Clin. Res. Ed.). 1988. Vol. 296. N 6622. P. 615-617.
- Muller-Lissner S. A. Obstipation // E. G. Hahn, J. F. Riemann, L. Demling. Ktinische Gastroenterologie, 3. Aufl., Georg. Thieme Verlag, 1996. P. 318-327.
- Pare P. The approach to diagnosis and treatment of chronic constipation: suggestions for a general practitioner // Can. J. Gastroenterol. 2011. N25. Suppl. В. Р. В36-40.
- PetticrewM., Watt L, Sheldon T. Systematic review of the effectiveness of laxatives in the elderly // Health Technol. Assess. 1997. Vol. 1. N 13. P. i-iv, 1-52.
- Pinto-Sanchez M. I, Bercik P. Epidemiology and burden of chronic constipation // Can. J. Gastroenterol. 2011. N25. P. 11-15.
- Ramkumar D., Rao S. S. Efficacy and safety of traditional medical therapies for chronic constipation: systematic review // Am. J. Gastroenterol. 2005. Vol. 100. N4. P. 936-971.
- Storr M., Storr M. Chronic constipation: current management and challenges // Can. J. Gastroenterol. 2011. N25. Suppl. В. Р. В5-6.
- Tramonte S. M., Brand M. В., Mulrow С D., Amato M. G. et al. The treatment of chronic constipation in adults. A systematic review // J. Gen. Intern. Med. 1997. Vol. 12. N1. P. 15-24.
- Voderholzer W. A., Schatke W., Muhldorfer В. Е., Klauser A. G. et al. Clinical response to dietary fiber treatment of chronic constipation // Am. J. Gastroenterol. 1997. Vol. 92. N1. P. 95-98.
- Voderholzer W. A., Schatke W., Muhldorfer В. Е., Klauser A. G. et al. Clinical response to dietary fiber treatment of chronic constipation // Am. J. Gastroenterol. 1997. Vol. 92. N 1. P. 95-98.
- Wald A. Approach to the patient with constipation // T. Yamada, D. H. Alpers, N. Kaptowitz et at. Textbook of Gastroenterology, 4’d ed. McGraw-Hill Med. Pub., 2003. Vol. 1. P. 894-910.
- Wald A. Slow Transit Constipation // Curr. Treat. Options Gastroenterol. 2002. Vol. 5. N 4. P. 279-283.
Статья опубликована на сайте http://www.gastroscan.ru
материал MedLinks.ru







