Гипотеза о том, что ингибирование фермента дипептидилпептидазы 4-го типа (ДПП-4) может представлять собой новый подход к лечению сахарного диабета 2 типа (СД2), впервые была опубликована в 1995 г. [1–3]. Механизм действия, описанный Диконом и коллегами [1], представлял собой специфическое ингибирование физиологического ферментативного расщепления глюкагоноподобного пептида 1 (ГПП-1) и глюкозозависимого инсулинотропного полипептида (ГИП), что приводило к накоплению биологически активных форм обоих гормонов. Доступность ингибиторов ДПП-4 (иДПП-4), таких как валинпирролидид [4], позволила подтвердить концепцию на животных моделях СД2 [5]. Целью концепции ингибирования ДПП-4 было создание препарата, который обладал бы сахароснижающей способностью с относительной свободой от риска гипогликемии благодаря глюкозозависимому инсулинотропному эффекту инкретиновых гормонов [6].
С 2006 г., когда иДПП-4 вошли в клиническую практику, они начали широко использоваться не только в качестве второго препарата в комбинации с метформином, но и в качестве монотерапии при плохой переносимости первого, а также в комбинации с остальными группами противодиабетических средств.
Ингибиторы ДПП-4 оказывают свое сахароснижающее действие косвенно, в результате быстрого распада и инактивации ГПП-1 и ГИП. За счет увеличения интактных и биологически активных последовательностей обоих пептидов высвобождается инсулин и, в случае ГПП-1, подавляется высвобождение глюкагона глюкозозависимым образом [6]. Обращают на себя внимание два аспекта этого явления. Во-первых, снижается риск гипогликемии, поскольку оба инкретиновых гормона влияют только на высвобождение инсулина и глюкагона в зависимости от уровня глюкозы [6]. Во-вторых, терапия на основе инкретинов является единственной способной в настоящее время устранить дефект α-клеток при СД2, при котором патофизиологически повышена выработка глюкозы печенью [7]. Снижение риска гипогликемии является явным преимуществом по сравнению с использованием препаратов сульфонилмочевины (ПСМ) [8].
Ингибиторы ДПП-4 — вещества с низкой молекулярной массой, благодаря чему, с одной стороны, обеспечивается относительно простое производство, с другой стороны, в сравнении с препаратами на основе пептидов они характеризуются гораздо меньшей вероятностью патологических иммунных реакций. К основным особенностям молекул с низкой молекулярной массой можно отнести следующие [9]:
-
высокое всасывание при приеме внутрь, а также хорошие фармакокинетические профили без использования усилителей всасывания;
-
соизмеримость с желаемой абсорбцией, распределением во внеклеточном пространстве, метаболизмом лекарственного средства и свойствами его выведения;
-
минимизация любого чрезмерного метаболизма лекарственного средства in vivo;
-
селективность по отношению к фармакологической мишени в сравнении с неспецифической или нецелевой активностью;
-
возможность использования препарата в виде таблеток как в качестве отдельного компонента, так и в качестве составной части комбинации фиксированных доз с обычно применяемыми совместно препаратами (например, с метформином);
-
эффективное снижение уровня глюкозы по сравнению с альтернативными средствами при использовании разумных дозировок.
Глюкозозависимый инсулинотропный полипептид вносит определенный вклад в эффективность снижения уровня глюкозы при отсутствии риска гипогликемии [10], что указывает на один из важных аспектов механизма действия ингибиторов фермента: включение в работу более одного эндокринного медиатора может повлиять на их терапевтические эффекты. Это еще больше отличает иДПП-4 от других препаратов, используемых для лечения СД2, которые могут различным образом воздействовать на разные системы органов, тем самым увеличивая риск появления нежелательных лекарственных реакций.
Существует немалый интерес к разработке двойных агонистов инкретинов ГПП-1 и ГИП, и FDA не так давно одобрило первый инкретин двойного действия (тирзепатид)1, однако, возможно, иДПП-4 следует рассмотреть как прагматичную альтернативу таким гибридным молекулам, по крайней мере в том, что касается эндокринного механизма действия. В случае иДПП-4 было показано, что лекарства влияют на очень немногие субстраты с физиологической точки зрения [11], и первоначальные опасения, что иДПП-4 могут повлиять на несколько эндокринных систем, что увеличит риск побочных эффектов, обусловленных механизмом действия, оказались неподтвержденными [12].
Было показано, что сахароснижающая эффективность иДПП-4 значимо не уступает другим широко используемым перорально противодиабетическим средствам, в том числе метформину и ПСМ [11, 13]. Также было показано, что эффект снижения уровня глюкозы иДПП-4 в значительной степени дополняет эффект большинства других пероральных сахароснижающих средств (ПССП). [11]. Более того, иДПП-4 доказали свою эффективность в качестве ПССП, снижающих уровень глюкозы в крови на каждом этапе лечения СД2: от применения в качестве препарата первой линии до комбинации с базальным инсулином [11]. В дополнение к их эффективности иДПП-4 также могут быть включены в состав комбинированных таблеток с фиксированной дозой.
В целом иДПП-4 характеризуются следующими особенностями [13]:
-
глюкозозависимая стимуляция секреции инсулина;
-
глюкозозависимое подавление секреции глюкагона;
-
снижение продукции глюкозы печенью;
-
отсутствие влияния на моторику желудка;
-
нейтральное действие на массу тела;
-
потенциальный протективный эффект в отношении β-клеток.
Хорошо известно, что индивидуальный подход к каждому пациенту является приоритетным при выборе тактики лечения. Изменение образа жизни (рациональное питание и повышение физической активности) и обучение принципам управления заболеванием являются неотъемлемой частью лечения СД. При инициации терапии и далее на любом этапе лечения необходимо оценивать индивидуальные характеристики пациента и выделять доминирующую клиническую проблему. Особенно следует учитывать высокий риск ассоциированных сердечно-сосудистых заболеваний, а также гипогликемий, влияние на массу тела. При этом стартовая комбинированная терапия метформином и иДПП-4 имеет преимущества по сохранению инсулин-секреторной функции [13].
В настоящее время на территории Российской Федерации зарегистрированы следующие препараты из группы иДПП-4: ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин, алоглиптин, гозоглиптин, гемиглиптин, эвоглиптин, из которых только гозоглиптин — единственный препарат на рынке, полностью локализованный в РФ, включая производство субстанции.
Группа иДПП-4 несколько неоднородна: для большинства препаратов возможно применение на всех стадиях хронической болезни почек (ХБП) с соответствующим снижением дозы; без снижения дозы применяют линаглиптин и гемиглиптин (включая стадию С5), эвоглиптин (включая стадию С4). С осторожностью используют при тяжелой печеночной недостаточности (кроме саксаглиптина, линаглиптина), хронической сердечной недостаточности.
Результаты многоцентрового рандомизированного исследования (n=299, возраст пациентов 27–77 лет, продолжительность наблюдения 9 мес. (36 нед.)) показали, что гозоглиптин является эффективным и безопасным сахароснижающим препаратом и в настоящее время может быть рекомендован пациентам с СД2 в дозе 30 мг/сут как в качестве монотерапии, так и в комбинации с другими ПССП [14, 18] (рис. 1–3).
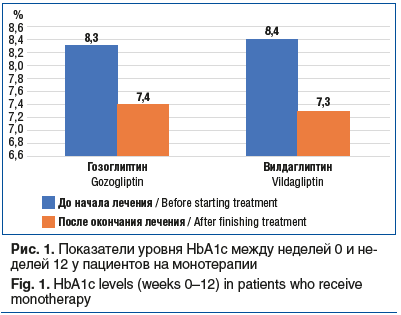
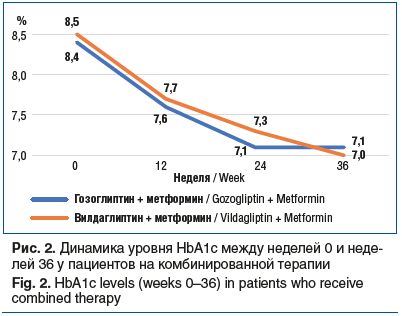
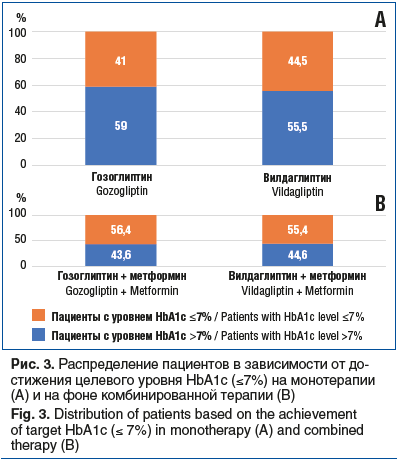
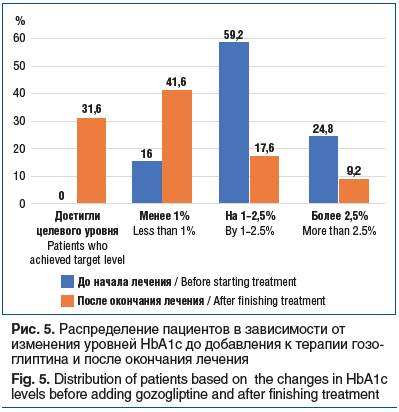
Другое исследование, уже из реальной клинической практики, — ОНИКС, также было посвящено изучению клинической эффективности гозоглиптина (Сатерекс®). В исследование включали пациентов, получавших стандартную терапию метформином и не достигавших рекомендованных показателей уровня глюкозы и HbA1c. Всего был обследован 1231 пациент в возрасте от 34 до 84 лет, а длительность наблюдения составила 6 мес. На фоне применения гозоглиптина треть пациентов достигла целевого уровня HbA1c, уровень HbA1c в целом по группе снизился с 8,39 до 7,29%, значительно сократилось количество пациентов с высоким уровнем превышения показателей гликемии (рис. 4, 5) [15].
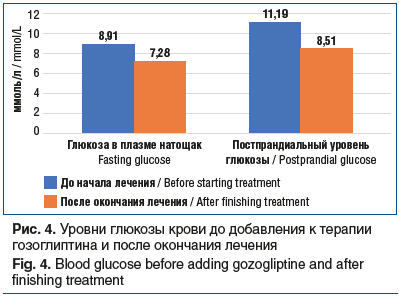
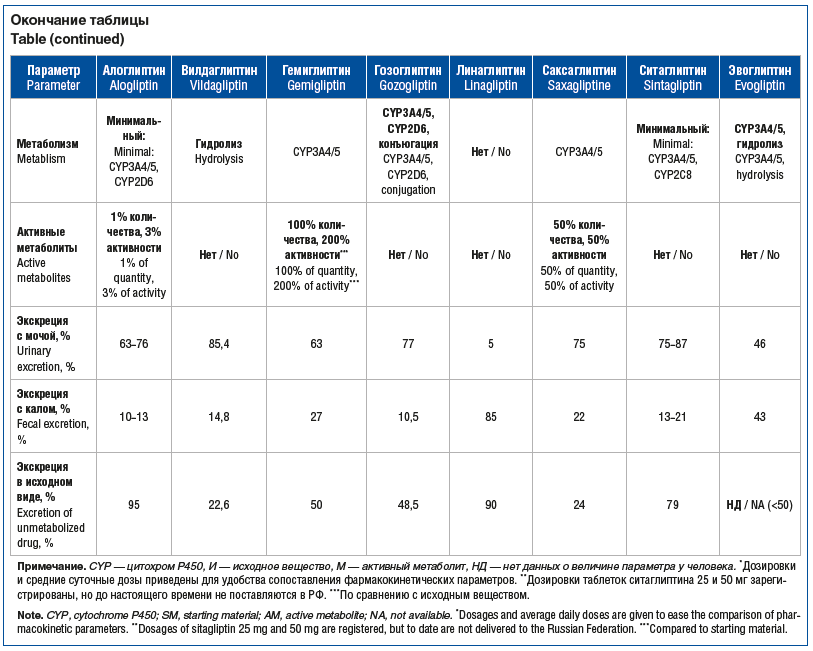
Как видно из таблицы, гозоглиптин является высокоселективным препаратом, и ингибирование ДПП-4 происходит на 80% и более через 1 сут после приема одной терапевтической дозы. На сегодняшний день производится и в клинической практике используется только одна дозировка 30 мг. Препарат обладает высокой биодоступностью среди представителей иДПП-4, и она не зависит от приема пищи.
![Таблица. Сравнительный обзор клинической фармакологии иДПП-4 [16] Table. Comparative analysis of DPP-4 inhibitors [16] Таблица. Сравнительный обзор клинической фармакологии иДПП-4 [16] Table. Comparative analysis of DPP-4 inhibitors [16]](https://medblog.su/wp-content/uploads/2023/12/1702249717_233_Vklad-ingibitorov-dipeptidilpeptidazy-4-go-tipa-v-realnuyu-praktiku-upravleniya-saharnym.png)
Поскольку гозоглиптин не является субстратом микросомальных ферментов печени, а также не ингибирует и не индуцирует эти ферменты, взаимодействие гозоглиптина с лекарственными средствами, которые являются субстратами, ингибиторами или индукторами микросомальных ферментов печени, маловероятно.
Клинически значимого взаимодействия гозоглиптина с лекарственными средствами, наиболее часто применяемыми при лечении СД2, не установлено.
Важными преимуществами гозоглиптина являются удобство применения (1 р/сут) и низкая частота гипогликемий, доступность для пациентов. У пациентов с ХБП легкой степени уменьшение дозы не требуется, и возможно применение при скорости клубочковой фильтрации более 45 мл/мин/1,73 м2. У пожилых пациентов коррекция дозы не требуется [17].
Таким образом, благодаря полному циклу производства препарата на территории нашей страны обеспечивается экономически и логистически доступное лечение пациентам с СД2. Согласно Алгоритмам специализированной медицинской помощи больным сахарным диабетом (2023 г.) [13] с момента постановки диагноза СД2 отдается предпочтение ранней комбинированной терапии заболевания, и иДПП-4 присутствуют на всех этапах лечения. Подобная терапия позволяет осуществить не только длительное эффективное, но и безопасное управление СД2 с достижением целевых показателей глюкозы, воздействием на ключевые звенья патогенеза диабета, рядом плейотропных эффектов (к примеру, нефропротекцией и замедлением прогрессирования диабетической нейропатии за счет снижения интенсивности воспаления и окислительного стресса, потенциальным кардиопротективным действием, иммуномодулирующим эффектом) [19, 20], позволяя защитить пациента от развития поздних макро- и микрососудистых осложнений заболевания.
Сведения об авторах:
Черникова Наталья Альбертовна — к.м.н., доцент кафедры эндокринологии ФГБОУ ДПО РМАНПО Минздрава России; 125993, Россия, г. Москва, ул. Баррикадная, д. 2/1; врач-эндокринолог ЦКБ ГА; 125367, Россия, г. Москва, Иваньковское ш., д. 7; ORCID iD 0000-0002-0562-8396.
Кнышенко Ольга Андреевна — врач-эндокринолог ЦКБ ГА; 125367, Россия, г. Москва, Иваньковское ш., д. 7; ORCID iD 0000-0003-0501-0307.
Контактная информация: Черникова Наталья Альбертовна, e-mail: nachendoc@yandex.ru.
Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов: отсутствует.
Статья поступила: 19.07.2023.
Поступила после рецензирования: 11.08.2023.
Принята в печать: 05.09.2023.
About the authors:
Natal’ya A. Chernikova — C. Sc. (Med.), associate professor of the Department of Endocrinology, Russian Medical Academy of Continuous Professional Education; 2/1, Barrikadnaya str., Moscow, 125993, Russian Federation; endocrinologist, Central Clinical Hospital of Civil Aviation; 7, Ivan’kovskoe road, Moscow, 125367, Russian Federation; ORCID iD 0000-0002-0562-8396.
Olga A. Knyshenko — endocrinologist, Central Clinical Hospital of Civil Aviation; 7, Ivan’kovskoe road, Moscow, 125367, Russian Federation; ORCID iD 0000-0003-0501-0307.
Contact information: Natal’ya A. Chernikova, e-mail: nachendoc@yandex.ru.
Financial Disclosure: no authors have a financial or property interest in any material or method mentioned.
There is no conflict of interest.
Received 19.07.2023.
Revised 11.08.2023.
Accepted 05.09.2023.
1 Mounjaro FDA Approval History. (Electronic resource.) URL: https://www.drugs.com/history/mounjaro.html (access date: 12.09.2023).
Информация с rmj.ru





