Роль и место интраназальных кортикостероидов в лечении аллергического ринита на современном этапе
связи с БА, обусловлена его тесной связью с заболеваниями ЛОР-органов, такими как острый и хронический риносинусит, экссудативный средний отит [4, 5].
АР характеризуется иммунологически обусловленным (как правило, IgE-опосредованным) воспалением слизистой оболочки полости носа, вызванным причинно-значимым аллергеном и клинически проявляющимся ежедневно на протяжении не менее часа двумя и более симптомами: обильной ринореей, затруднением носового дыхания, зудом в полости носа, частым чиханьем и, нередко, аносмией [1, 3]. Заболевание может сопровождаться также экстраназальными симптомами (глазными, головной болью, гипоксией, постназальным затеком, кашлем и т. д.) [3].
Причиной АР являются экзоаллергены: пыльцевые, бытовые, эпидермальные, грибковые.
Содержание статьи
Классификация аллергического ринита
В зависимости от этиологического фактора выделяют сезонный, круглогодичный (бытовой), профессиональный АР [1]. Сезонный АР (САР) возникает при сенсибилизации (повышенной чувствительности) к пыльцевым и грибковым аллергенам: пыльце деревьев, злаковых и сорных трав, спорам грибов Cladosporium, Penicillium, Alternaria, Aspergillus и др. Круглогодичный АР (КАР) обусловлен сенсибилизацией к аллергенам клещей домашней пыли (Dermatophagoides pteronyssinus и Dermatophagoides farinae), библиотечной пыли, эпидермальным аллергенам животных и птиц, аллергенов плесневых грибков, тараканов, пищевых продуктов и др. [6–9].
Классификация международных согласительных документов по АР [1] предлагает разделять АР по характеру течения на интермиттирующий АР (ИАР), при котором симптомы беспокоят менее 4 дней в неделю или менее 4 нед. в году, и персистирующий АР (ПАР), при котором симптомы беспокоят более 4 дней в неделю и более 4 нед. в году [3]. При этом ИАР и ПАР не являются эквивалентами САР и КАР.
Лечение аллергического ринита
За последнее десятилетие принят ряд международных и национальных согласительных документов [1, 3, 10], согласно которым лечение АР обязательно включает проведение мероприятий по элиминации причинно-значимого аллергена, рациональную фармакотерапию, иммунотерапию, образовательные программы для пациентов [3, 10, 11]. Согласно новой парадигме целью лечения АР является полный контроль симптомов заболевания [1, 3]. В лечении АР предусмотрена 4-ступенчатая терапия, основанная на контроле симптомов [1]. Критерии контроля оценивают за последние 4 нед., любое отклонение рассматривается как утрата контроля. В этом случае может быть применена терапия step-up (ответ оценивают в течение 2 нед., если нет ответа, переходят на следующую ступень) [3].
Основу фармакотерапии АР составляют системные и интраназальные Н1-блокаторы II поколения (антигистаминные препараты — АГП) — препараты первого выбора у пациентов с легкими симптомами САР и КАР, а также топические интраназальные кортикостероиды (ИнКС), назначаемые при среднетяжелой и тяжелой форме заболевания и при отсутствии эффекта от проводимой терапии на первой ступени лечения [1, 3, 8, 12–17] (табл. 1).![Таблица 1. Сравнительная характеристика лекарственных средств для лечения АР [17] Таблица 1. Сравнительная характеристика лекарственных средств для лечения АР [17]](https://medblog.su/wp-content/uploads/2019/06/rol-i-mesto-intranazalnyh-kortikosteroidov-v-lechenii-allergicheskogo-rinita-na-sovremennom-etape-churyukina-e-v.png)
Место ИнКС в лечении аллергического ринита
С начала 1970-х гг. ИнКС зарекомендовали себя как эффективное средство лечения АР. ИнКС могут быть использованы как в монотерапии, так и в комбинации с пероральными АГП [18]. Кохрейновский метаанализ показал, что при длительном применении ИнКС имеют преимущество над АГП [19]. Рекомендации специалистов из США и большинства европейских государств определяют ИнКС как первую линию терапии при среднетяжелом и тяжелом АР [1, 3]. В 2017 г. экспертная группа внесла изменения в международный согласительный документ ARIA (Allergic Rhinitis and its Impacton Asthma — Аллергический ринит и его влияние на астму). Изменения коснулись фармакотерапии АР. Так, указано, что при САР: рекомендуется комбинация ИнКС и перорального АГП или монотерапия ИнКС; комбинация ИнКС и интраназального блокатора H1-гистаминового рецептора предпочтительней, чем монотерапия последним; рекомендуется либо антагонист лейкотриеновых рецепторов, либо пероральный АГП [3]. При КАР: предпочтительней терапия ИнКС, чем комбинация ИнКС с пероральным АГП; пероральный АГП предпочтительней антагониста лейкотриеновых рецепторов [3]. Общие рекомендации по лечению пациентов с САР и КАР: рекомендуется комбинация ИнКС и интраназального АГП или ИнКС; предпочтительней терапия ИнКС, чем введение интраназального АГП; рекомендуется введение либо интраназального, либо перорального АГП [3].
Механизм действия постоянно изучается. В экспериментальных и клинических исследованиях показано, что глюкокортикостероиды (ГКС) воздействуют практически на все этапы патогенеза АР [20, 21]. Их терапевтический эффект при АР связывают, прежде всего, с противовоспалительным и десенсибилизирующим действием. Преимуществом ИнКС перед пероральными кортикостероидами является минимальный риск системных побочных эффектов на фоне адекватных концентраций активного вещества в слизистой оболочке носа, позволяющих контролировать симптомы АР, как назальные, так и глазные [21, 22]. Последнее обусловлено торможением назоокулярного рефлекса за счет выраженной локальной противовоспалительной активности интраназальных стероидов [22].
ИнКС обладают высокой эффективностью, быстротой наступления и продолжительностью лечебного действия, высоким профилем безопасности [21–23]. Сегодня в распоряжении врача имеется широкий выбор ИнКС: беклометазона дипропионат, будесонид, флутиказона фуроат, флутиказона пропионат, мометазона фуроат [24]. Дозы и режимы их применения представлены в таблице 2 [25].
При выборе ИнКС следует учитывать их фармакодинамические (сродство к ГКС-рецепторам), физико-химические (липофильность) и фармакокинетические (системная биодоступность) свойства, а также степень их изученности в адекватных клинических исследованиях [26]. Сродство к ГКС-рецепторам определяет силу действия препарата, липофильность — степень и скорость его проникновения через клеточные мембраны, достижение ГКС-рецептора и длительность пребывания в слизистой оболочке носа, а системная биодоступность — частоту развития нежелательных эффектов, переносимость и, как следствие, приверженность лечению [27].![Таблица 2. Дозы и режимы применения препаратов современных ИнКС [25] Таблица 2. Дозы и режимы применения препаратов современных ИнКС [25]](https://medblog.su/wp-content/uploads/2019/06/1560298542_995_rol-i-mesto-intranazalnyh-kortikosteroidov-v-lechenii-allergicheskogo-rinita-na-sovremennom-etape-churyukina-e-v.png)
При применении разных методов оценки сродства к ГКС-рецепторам беклометазона дипропионат (БДП), будесонид (БУД), дексаметазон (ДМ), мометазона фуроат (МФ), триамцинолон (ТРИАМ), флутиказона пропионат (ФП), флутиказона фуроат (ФФ), флунизолид (ФЛУ, не зарегистрирован в РФ), циклесонид (ЦИК) располагались в следующей последовательности: ФФ > МФ > ФП > ТРИАМ > БУД > ДМ [28] или ФП > МФ > БУД > ФЛУ > ТРИАМ [29]. Липофильность ГКС (logP) и растворимость (мкг/мл) соответственно были равны: у МФ — 5,5 и
Клиническую эффективность и безопасность ИнКС обеспечивают такие физические параметры, как: 1) депозиция (зависит от вязкости, невязкая жидкость распределяется лучше — до 99%); 2) абсорбция (зависит от размера частиц и липофильности); 3) клиренс (скорость элиминации обратно пропорциональна вязкости; с учетом скорости движения ресничек мерцательного эпителия слизистой верхних дыхательных путей (6 мм/мин) быстрее устраняется невязкая жидкость) [26]. Исходя из этого идеальным может считаться назальный спрей с суспензией, имеющей высокую депозицию и высокую вязкость. Этот парадокс может быть преодолен тиксотропностью суспензии ИнКС — способностью снижать вязкость при встряхивании (Па˙с) [26, 33]. Таким образом, высокий аппликационный эффект в полости носа обеспечивается высокой начальной и конечной вязкостью [33]. По этой характеристике лидирует мометазона фуроат: 58,6 (Па˙с), в то время как у беклометазона дипропионата этот показатель составляет 3,5 (Па˙с) [26].
Наиболее низкая биодоступность (менее 0,1%) характерна для мометазона фуроата [34, 35], что обусловливает низкий риск развития системных нежелательных реакций при его применении. Системная биодоступность других ГКС при интраназальном введении колеблется от менее чем 2% у флутиказона пропионата до 10% у будесонида, от 44% у беклометазона до более чем 80% у дексаметазона [34, 35]. Согласно результатам большого систематического обзора мометазона фуроат обладает отличным профилем безопасности, он не вызывает побочных эффектов, характерных для ГКС системного действия, не подавляет функцию коры надпочечников, не влияет на скорость роста у детей, безопасен для матери и плода при применении во время беременности [35]. При длительном использовании препарата не отмечено изменений толщины эпителия и атрофии слизистой оболочки [35
Профиль безопасности ГКС определяется также их воздействием на геном либо клеточную мембрану или мембраносвязанные кортикоидные рецепторы. Геномный механизм, открытый в 1970-е гг., заключается в связывании ГКС с ГКС-рецепторами в цитоплазме. Образовавшийся комплекс «глюкокортикоид — глюкокортикоидный рецептор» транспортируется в ядро, где он активирует экспрессию генов, отвечающих за синтез противовоспалительных антигенов [14, 29–32]. Открытый же относительно недавно внегеномный механизм включает непосредственное ингибирование комплексами «глюкокортикоид — глюкокортикоидный рецептор» факторов транскрипции провоспалительных антигенов [28]. Благодаря тому что у мометазона фуроата преобладает внегеномный механизм, по сравнению с другими ГКС противовоспалительный эффект развивается быстрее, а влияние на геном сведено к минимуму, что во многом обусловливает его высокий профиль безопасности [35].
Несмотря на появление новых современных препаратов, длительное время не удавалось достоверно сравнить эффективность применения ИнКС. Немецкими учеными был разработан такой метод и найдена величина, названная TIX (Therapeutic index — терапевтический индекс), которая определяется как соотношение суммарной эффективности по 3 показателям эффективности (общему баллу назальных симптомов, общему баллу глазных симптомов, общей оценке пациентами) и суммарной безопасности кортикостероида по 3 показателям безопасности (частоте возникновения эпистаксиса — носовых кровотечений, влиянию на уровень кортизола, глазным нежелательным явлениям — повышению внутриглазного давления и возникновению катаракты) [36]. В таблице 3 приведены терапевтические индексы, разработанные на основании метаанализа 84 исследований для 6 действующих веществ [36].
Таким образом, при систематическом обзоре данных все рассмотренные ИнКС доказанно продемонстрировали эффективность и безопасность. Максимальный терапевтический индекс, отражающий максимальную эффективность и минимальное количество нежелательных явлений при лечении АР, выявлен у мометазона фуроата [36].
Назальный спрей мометазона фуроата изучался более чем в 300 клинических исследованиях [35], в которых была показана его эффективность и безопасность при САР и КАР, остром и хроническом риносинусите, гипертрофии аденоидов и среднем отите у детей [37]. Его безопасность показана не только в рандомизированных клинических исследованиях, но и подтверждена опытом более чем 20-летнего применения в широкой медицинской практике [11, 33]. При АР рекомендуется применение спрея мометазона фуроата в дозе 50 мкг в каждую половину носа 1 р./сут в течение 1–6 мес. и более [35], что обычно позволяет на 24 ч купировать все симптомы АР, включая заложенность носа. Мометазона фуроат начинает действовать уже в течение 7–12 ч после приема первой дозы, имеет хороший профиль безопасности, а при длительном применении не сушит слизистую носа, но способствует восстановлению ее нормальной структуры. Высокий профиль безопасности препарата позволяет использовать его у детей с 2-летнего возраста [35].
В 2016 г. в РФ был выпущен и зарегистрирован первый российский глюкокортикоид в форме назального спрея — Нозефрин® (АО «Вертекс»). В данный момент Нозефрин® — единственный российский спрей на основе мометазона фуроата. Нозефрин® обладает всеми преимуществами мометазона фуроата как топического ГКС: высокой противовоспалительной активностью, обусловленной тропностью к эпителию слизистой оболочки полости носа, хорошей растворимостью в назальном секрете, минимальным системным и местным побочным действием благодаря низкой биодоступности (в терапевтических дозах может применяться длительно, более полутора лет). Комплексный механизм противовоспалительного действия препарата Нозефрин® обусловливает многообразие показаний к его применению, включая: САР и КАР, острый синусит или обострение хронического синусита, полипоз носа [38].
Среди других спреев мометазона фуроата Нозефрин® выделяется длительным сроком годности (3 года), удобной упаковкой, которая обеспечивает качественное распыление препарата и орошение слизистой оболочки носа на протяжении всего срока годности. Для этого в дозаторе (фирма Aptar Radolfzell GmbH, Германия) есть специальные приспособления: уплотненный наконечник, предотвращающий засорение; фильтрующая мембрана, которая фильтрует обратный поток воздуха после нажатия; металлическая пружина, не контактирующая с содержимым флакона и не окисляющаяся (рис. 1).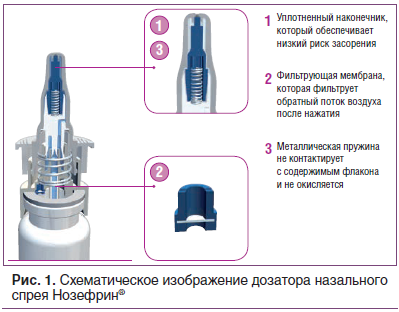
![Таблица 3. Терапевтический индекс для параметров, баллов и заключительного соотношения по каждому действующему веществу (адаптировано из [36]) Таблица 3. Терапевтический индекс для параметров, баллов и заключительного соотношения по каждому действующему веществу (адаптировано из [36])](https://medblog.su/wp-content/uploads/2019/06/1560298543_862_rol-i-mesto-intranazalnyh-kortikosteroidov-v-lechenii-allergicheskogo-rinita-na-sovremennom-etape-churyukina-e-v.png)
Таким образом, российский препарат мометазона фуроата Нозефрин® не уступает по качеству своим иностранным аналогам.
Нами было проведено проспективное открытое наблюдательное несравнительное исследование, целью которого была оценка эффективности, переносимости и безопасности интраназального спрея Нозефрин® у больных САР в сочетании с аллергическим конъюнктивитом или без такового. В исследование были включены 55 пациентов, страдающих САР в стадии обострения, проходящих лечение второй ступени и более, с историей заболевания не менее 2 лет. Средний возраст пациентов составил 23,7±5,2 года (от 12 до 52 лет). Средняя длительность заболевания составила 10,63±4,1 года (от 2 до 16 лет). Исследование продолжалось 6 мес. (май — октябрь 2018 г.), период терапии и активного наблюдения — 28 дней. Пациенты имели сенсибилизацию преимущественно к аллергенам сорных трав, реже — к аллергенам злаков, луговых трав, пыльцы деревьев. Данные кожного тестирования, проведенного в ремиссии заболевания, согласовывались с анамнезом и пиком клинических проявлений у пациентов. Эффективность препарата оценивалась по динамике 6 критериев: 1) симптомы АР назальные; 2) симптомы АР глазные; 3) симптомы, характеризующие качество жизни, определяемые с помощью модифицированного валидизированного опросника Rhinoconjunctivitis Quality of Life Questionnaire (RQLQ) [3, 7–9, 17]; 4) уровень эозинофилов в назальном секрете (определяется по риноцитограмме); 5) уровень эозинофилов в периферической крови; 6) общая эффективность терапии, оцененная пациентами при заполнении анкеты и отдельно оцененная врачом-исследователем по окончании исследования. Выраженность симптомов АР оценивалась по интегральному индексу симптомов от 0 до 3 баллов [3, 7–9, 17], который включает оценку назальных симптомов АР по шкале Total nasal symptom score (Общая шкала назальных симптомов) и неназальных симптомов АР по шкале Total Non Nasal Symptom Score (Общая шкала неназальных симптомов). Безопасность препарата оценивалась на основании субъективных жалоб пациента, данных физикального и лабораторного обследования, отсутствия побочных эффектов и осложнений.
Положительный клинический эффект получен у 48 (87,3%) пациентов, использовавших назальный спрей Нозефрин® в виде монотерапии, из них отличный результат отмечен у 18 (37,5%) пациентов, хороший результат — у 26 (54,2%) и удовлетворительный результат — у 4 (8,3%). У 7 (12,7%) больных с тяжелыми проявлениями АР эффект был признан недостаточным при монотерапии препаратом Нозефрин®, им дополнительно были назначены Н1-блокаторы либо эти же Н1-блокаторы в сочетании с антагонистами лейкотриеновых рецепторов. Выявлена выраженная положительная динамика изменения показателей качества жизни (согласно опроснику RQLQ) пациентов с САР (n=55) на фоне проводимой терапии: средний балл составил 21,6±18,3 (снижение относительно исходных данных на 86,4 балла, т. е. на 80,1%). Ни один пациент не отметил отсутствия эффекта или ухудшения состояния, не имел неприятных ощущений при использовании назального спрея Нозефрин®, не предъявил жалоб на носовые кровотечения, сухость либо жжение в носу, образование корочек и др. На протяжении всего периода лечения спреем Нозефрин® не отмечено отрицательной динамики показателей общеклинического анализа. Все 55 пациентов закончили курс лечения (28 дней) полностью, в т. ч. пациенты, у которых клинический эффект был недостаточным и которым было назначено дополнительное лечение. Все это свидетельствует о хорошей переносимости препарата.
Заключение
Таким образом, в настоящем исследовании у 87,3% пациентов с САР показана хорошая клиническая эффективность и безопасность отечественного назального спрея Нозефрин® (действующее вещество мометазона фуроат) в монотерапии, что подтверждено объективными данными и субъективной оценкой самих пациентов. Высокая эффективность ИнКС обусловлена их выраженным противовоспалительным действием, благодаря которому они зарекомендовали себя самыми эффективными препаратами в лечении АР среднетяжелой и тяжелой формы. Интраназальный спрей мометазона фуроата Нозефрин® может быть препаратом выбора в терапии АР.
В заключение еще раз подчеркнем, что АР требует эффективного лечения не только при острой симптоматике в сезон обострения, но также при персистирующем течении и при сочетании с другими аллергическими проявлениями. Современные руководства рекомендуют для лечения АР ИнКС в качестве основных препаратов, поскольку они эффективны и безопасны, просты в использовании, предоставляют возможность выбора с учетом индивидуальных предпочтений, что повышает приверженность пациентов лечению.
Информация с rmj.ru





